Manuel Corpas
El director del Curso en Experto en Genética Clínica y Medicina Personalizada de UNIR, Manuel Corpas, profundiza en torno a algunas ideas sobre el impacto de la genómica en la medicina del futuro.

Si analizamos a los países industrializados y prevemos cómo evolucionará su población, nos encontramos con un envejecimiento generalizado de la población y, por lo tanto, con una gran demanda de recursos médicos para el tratamiento y el diagnostico de enfermedades, principalmente aquellas que presentan un mayor índice de mortalidad en estos países.
Medicina personalizada o medicina de precisión
El envejecimiento de la población conlleva una gran demanda de recursos en los sistemas sanitarios, pero disponemos de unos presupuestos restringidos. Hay que, por lo tanto, innovar con lo que tenemos para mejorar la salud de la población.
Como vemos en la siguiente gráfica, el porcentaje de personas mayores de 65 años sigue aumentando, mientras se estanca el porcentaje del PIB destinado a sanidad.
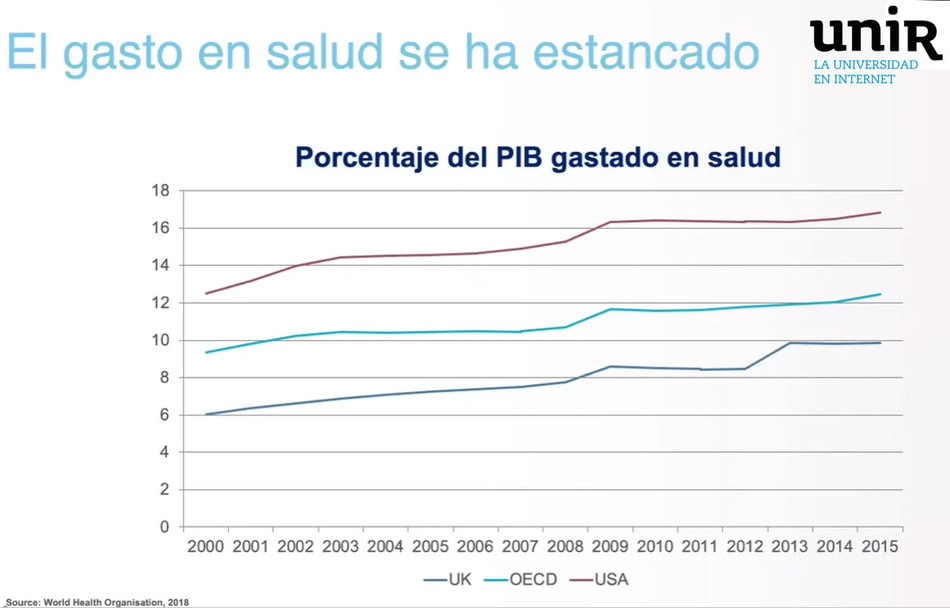
Hay que racionalizar como nunca antes los recursos para disponer de una medicina más precisa y personalizar diagnósticos, tratamientos, medicamentos. Una medicina predictiva, personalizada, preventiva.
Cómo optimicemos la medicina determinará su futuro
La genómica es la nueva revolución médica. Permite caracterizar todas las funciones de todos los genes en la genoma humana. Toda enfermedad, en un porcentaje mayor o menor, está influenciada por la genética. Es decir, la susceptibilidad de padecer enfermedades, y todos los rasgos que se observan en los pacientes, tienen una condición genética importante.
La genómica nos permitirá tener una medicina precisa, basada en la evidencia, dirigida y estratificada, que influya antes y después de que aparezcan los síntomas y que esté basada en los riesgos genéticos del individuo. Todo ello es posible porque:
- Tenemos la capacidad de producir datos genómicos de forma más barata y accesible. Esto tendrá un papel fundamental en la medicina preventiva.
- Podemos medir, gracias a los datos genéticos, en un punto hasta ahora impensable, aunque ya es una realidad.
Antes, sin la genómica, la medicina trabajaba mediante ensayo y error, medía igual a todos los individuos, era más generalista y aplicaba tratamientos tras la aparición de síntomas. Era prescriptiva, no preventiva. Ahora podemos prescribir mejor medicamentos, seleccionar éstos con más seguridad y eficacia desde el comienzo, y adecuar dosis con mayor rapidez.
Para demostrar esto de una manera más gráfica, en la siguiente imagen observamos en azul a la persona que ha consumido el fármaco con eficacia, comparada con la población en rojo que la recibió sin haber obtenido los beneficios esperados. Siempre se ha de tener en cuenta que son datos de una medicina prescriptiva y no personalizada.
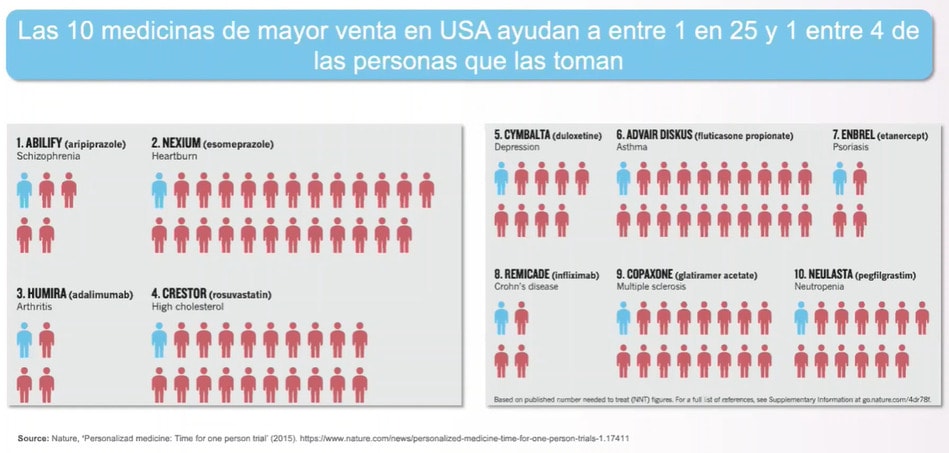
El papel de la genómica en la medicina del futuro
Toda la presencia de datos se sustenta en una serie de tecnologías basadas, a su vez, en el genoma humano. Podemos realizar diversos tipos de análisis:
- Array. Prueba con la que cubrimos hasta 100 millones de marcadores que dan una cobertura extensa a lo largo de todos los cromosomas, pero aún es insuficiente por la cantidad de cromosomas con los que contamos.
- Secuenciación del exoma. El gran avance de los últimos años. Ahora tenemos la capacidad de analizar marcadores específicos. Además, podemos reconstruir la secuencia de los pacientes. Consiste en tratar una muestra de ADN, trocearla en millones de fragmentos que se amplifican, determinar su frecuencia y reconstruirla, alineándola a un genoma de referencia. Esta recomposición del puzzle respecto al del paciente nos permite analizar millones de variaciones del paciente, lo que proporciona muchas coberturas.
- Secuenciación de genoma completo. Hacia donde se reconducen todos los análisis genéticos. Pero aún es cara, y resulta difícil manejar la gran cantidad de datos que se obtienen secuenciando, por ejemplo, unos 200 GB por paciente, como un disco duro de un ordenador completo. Su ventaja es que permite ver las variantes dentro y fuera de los genes, pero el coste es elevadísimo hoy en día.
El genoma completo permite la selección más extensa posible de análisis genéticos:
- Rastreo de patogenicidad: identificación de mutaciones monogénicas que probablemente sean patógenas.
- Puntaje de riesgo poligénico: la combinación ponderada de potencialmente millones de marcadores genéticos.
- Farmacogenómica: detecta la capacidad de un paciente para metabolizar fármacos y predice reacciones adversas.
- Análisis y fitness y nutrición. Identificación de marcadores para ayudar a optimizar los regímenes de dieta y ejercicio.
Caso de uso para contextualizar cómo la genómica puede prevenir enfermedades en los países industrializados, el potencial del puntaje de riesgo poligénico:
La gran mayoría de las muertes a día de hoy derivan de enfermedades complejas, como la arteriopatía cardiaca, la diabetes tipo 2 o la fibrilación atrial, entre otras. En el 2018, la revista Nature publicó el artículo Genome-wide polygenic scores for common diseases identify individuals with risk equivalent to monogenic mutations, a. Khera ET AL. en el que se mostró la predicción de riesgo a través de millones de marcadores para comprobar si dicho puntaje es capaz de discriminar a segmentos de una población de alto riesgos con respecto al resto de la población.
Por ejemplo, para arteriopatía cardiaca se observó que el 8% de casi 300.000 individuos tenían un alto riesgo, o superior de más de 3 veces que el resto para desarrollar esta enfermedad.
Identificación precoz de la arteriopatía coronaria
Los factores de riesgos convencionales no estaban presentes en la mayoría de los individuos que formaban parte de ese 8%. Factores como la hipertensión, la hipercolesterolemia o las enfermedades coronarias.
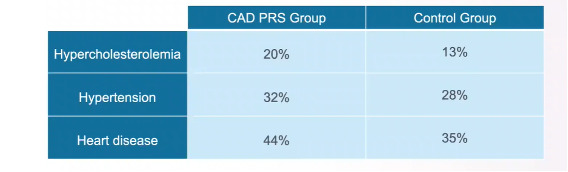
Un ejemplo práctico: el riesgo de desarrollar 27 enfermedades comunes en una familia de 4 individuos. En esta tabla podemos ver cómo hay riesgos de que los hijos hereden de ambos padres o solo de un progenitor.
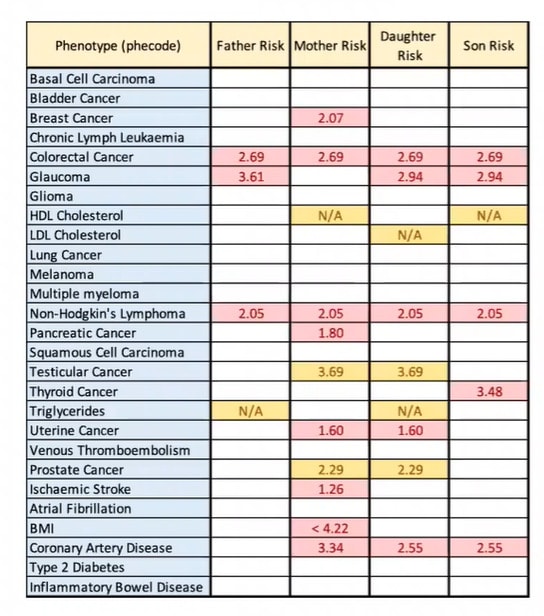
Las propensiones heredadas, como vemos en la tabla, puede producirse por un promedio de ambos progenitores. Mientras que, en este caso concreto, en cuanto al riesgo de enfermedad coronaria, la madre contribuye desproporcionadamente a elevar el riesgo de dicha patología en sus hijos.
Por lo tanto, el uso de la genética nos permite identificar riesgo de manera más temprana, antes incluso de que haya síntomas físicos Las intervenciones pueden dirigirse a prevenir esos riesgos sin esperar al desarrollo de la enfermedad.
En el caso de la familia anterior, tomándola como ejemplo, encontramos un hallazgo claro de mayor riesgo de arteriopatía coronaria, y un médico podría incorporar estrategias específicas de prevención y monitores de riesgos en un buen plan de gestión clínica.
Conclusiones
- El análisis genómico agrega una nueva dimensión en la prevención de enfermedades
- La secuenciación del genoma permite el análisis de. Screening de patogenicidad, puntaje de riesgo poligénico, farmacogenética y fitness y nutrigenómica.
- Utilizando daos de la genómica se pueden realizar intervenciones más precisas en individuos de alto riesgo.
Lo que aquí se ha analizado parte del conocimiento que se adquiere en el curso de genética clínica de UNIR, cuyos objetivos, entre otros, incluye adquirir una comprensión solida de la secuenciación de nueva generación (NGS); procesar, gestionar e interpretar dichos datos para prevenir la enfermedad; y conocer las fuentes de datos e implementar planes basados en la evidencia.
Puedes repasar la presentación aquí.
- Experto Universitario en Genética Clínica y Medicina Personalizada






